Một số hình ảnh của thuốc
Thuốc Osimertinib là một thuốc mới, Osimertinib lần đầu tiên được FDA chấp thuận vào 11/2015 và ở thời điểm đó nó chỉ được chỉ điều trị bước 2 sau khi bệnh tiến triển với TKI thế hệ I cho bệnh nhân NSCLC có đột biến EGFR và mang đột biến T790M. Sau đó hiệu quả của Osimertinib tiếp tục được khẳng định qua nghiên cứu AURA 3 là một nghiên cứu nhãn mở, pha 3 đa trung tâm với trên 400 bệnh nhân ung thư phổi không tế bào nhỏ có đột biến EGFR và mang đột biến T790M sau khi đã tiến triển với TKI bước 1. Nghiên cứu chia hai nhóm với tỷ lệ 2: 1 để bệnh nhân nhận Osimertinib (với liều 80mg mỗi ngày) hoặc Pemetrexed truyền tĩnh mạch (500 mg cho mỗi mét vuông da) cộng với Carboplatin AUC 5 hoặc cisplatin (liều 75mg mỗi mét vuông da) mỗi 3 tuần cho đến sáu chu kỳ; sau đó duy trì Pemetrexed
Kết quả nghiên cứu AURA 3:
Thời gian sống bệnh không tiến triển nhóm sử dụng Osimertinib dài hơn đáng kể so với điều trị Platinum kết hợp với Pemetrexed (10.1 tháng so với 4.4 tháng), Nghiên cứu phân tích dưới nhóm với các bệnh nhân có tổn thương di căn não. Trong số 144 bệnh nhân có tổn thương hệ thống thần kinh trung ương, thời gian sống bệnh không tiến triển trung bình ở nhóm dùng Osimertinib kéo dài hơn so với những bệnh nhân dùng Platinum kết hợp với Pemetrexed (8,5 tháng so với 4,2 tháng).

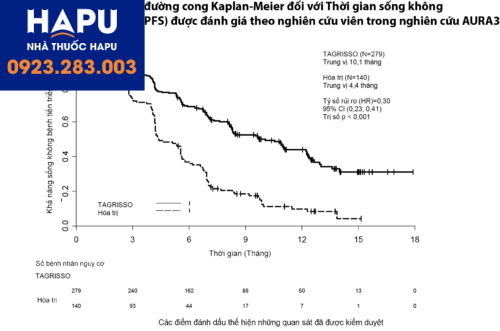

Kết luận nghiên cứu AURA 3:
Osimertinib có hiệu quả cao hơn đáng kể so với liệu pháp Platinum kết hợp với Pemetrexed ở những bệnh nhân ung thư phổi không tế bào nhỏ có đột biến T790M dương tính (bao gồm những người bị di căn thần kinh trung ương) trong bệnh đã tiến triển với liệu pháp TKI đầu tiên. Thời gian sống không bệnh trung vị đạt được 10.1 tháng, trên bệnh nhân có di căn não 11.7 tháng.
Trên đây là kết quả của nghiên cứu AURA 3 sử dụng thuốc biệt dược của Osimertinib (Tagrisso 80mg), thuốc Tagrix là thuốc generic, cùng chứa thành phần Osimertinib như Tagrisso 80mg. Hiện chưa có nghiên cứu cụ thể sử dụng thuốc Tagrix 80mg trên bệnh nhân ung thư phổi.
Cập nhật mới về Osimertinib thành phần trong thuốc Tagrix 80mg.
Mới cách đây không lâu vào 4/2018 bằng kết quả nghiên cứu FLAURA thuốc TKI thế hệ III này đã được FDA chấp thuận sử dụng cho bệnh nhân có đột biến EGFR ở exon 19 và 21 (không hề đề cập đến có hay không đột biến T790M)
Nghiên cứu FLAURA (1)
Thiết kế nghiên cứu về Osimertinib thành phần thuốc Tagrix 80 mg:
Nghiên cứu nhãn mờ, pha III, đa trung tâm với trên 500 bệnh nhân có đột biến gen EGFR ở exon 19 hoặc L858R trên exon 21 chưa được điều trị trước đó với các thuốc TKI. Các bệnh nhân phân nhóm theo tỷ lệ 1:1. Bệnh nhân có thể được sử dụng Osimertinib (với liều 80 mg một lần mỗi ngày) hoặc TKI tiêu chuẩn (Gefitinib với liều 250mg x 1lần/ngày hoặc Erlotinib với liều 150mg x 1lần/ngày)
Kết quả nghiên cứu:
Trung bình sống bệnh không tiến triển ở nhóm Osimertinib so với nhóm TKI tiêu chuẩn (18,9 tháng so với 10,2 tháng), thời gian duy trì đáp ứng trung bình 17,2 tháng với Osimertinib so với 8,5 tháng trong nhóm sử dụng TKI tiêu chuẩn.
Kết quả về thời gian sống thêm toàn bộ chưa được công bố tuy nhiên với số liệu ở thời điểm 18 tháng theo dõi nhóm bệnh nhân dùng Osimertinib có tỷ lệ sống còn đến 83% với và 71% trong nhóm TKI chuẩn.
Đó là những con số ấn tượng chứng minh hiệu quả ưu việt, mang đến thời gian sống thêm lâu hơn cho bệnh nhân của nhóm TKI thế hệ III.
Một số hình ảnh của thuốc Tagrix 80 mg


Nếu còn thắc mắc về thuốc Tagrix 80 mg hay bất cứ thuốc nào điều trị ung thư như: Thuốc Tagrix 80mg giá bao nhiêu tiền? Mua thuốc Tagrix ở đâu uy tín? Tagrix 80mg là thuốc gì? Công dụng, thành phần của thuốc Tagrix 80 mg là gì? Tác dụng phụ của thuốc Tagrix 80mg là gì? Biểu hiện khi bị tác dụng phụ của thuốc Tagrix 80mg? Thuốc điều trị ung thư có hiệu quả, an toàn? Vui lòng liên hệ với nhathuochapu.vn theo số hotline 0923 283 003 để được các Dược sĩ Đại học tư vấn một cách tận tâm nhất. nhathuochapu.vn xin chân thành cảm ơn quý khách hàng đã đọc bài viết: Thuốc Tagrix 80mg (Hộp 30 viên).
Nhận xét
Đăng nhận xét